|
차례 |
제 1장 |
제 2장 |
제 3장 |
제 4장 |
제 5장 |
제 6장 |
제 7장 | | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 자원과 환경: 지구의 선물, 그 빛과 그림자 - 제 2장 광물과 암석 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
2-1. 광물 2-2. 암석 2-3. 광물로 인한 환경 문제 2-4. 광상 2-5. 광해 2-6. 방사능과 환경 2-보충 학습 2-참고문헌 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
2-1. 광물 지구의 선물인 자원은 우리 주변을 둘러보면 참으로 많은 곳에 사용되고 있다. 자원은 크게 광물 암석 자원, 에너지 자원, 수자원으로 나눌 수 있다. 광물 자원에는 금속과 비금속 자원, 에너지 자원은 화석 연료와 핵연료 자원, 그리고 수자원은 지표수와 지하수 자원으로 나누어 볼 수 있다. 우리는 앞으로 이들 자원의 이용과 그로 인한 환경 문제들에 대해 하나씩 다룰 것이다. 우선은 이들 자원 중 광물, 암석 자원에 대해 먼저 살펴보도록 하자. 도시에 높아 솟아오른 건물을 짓는 콘크리트, 거리를 가득메운 자동차, 각 가정에 소중히 사용하는 자기 그릇들 이 모든 것이 광물로부터 만들어진 것이다. 이 외에도 광물이 사용되는 예는 무수히 많다. 2-1-1. 광물의 정의 및 생성 그렇다면 이런 광물은 도대체 무엇일까? 광물은 영어로 mineral이라고 하는데, 지질학에서 말하는 엄격한 의미에서의 광물은 다음과 같은 조건을 모두 만족하는 것이다.
광물이 되기 위해서는 첫 번째로 무생물적으로 만들어져야 한다. 예를 들면 조개가 만드는 진주 같은 것은 엄밀한 의미에서 광물이라 할 수 없다. 두 번째로는 자연산이어야 한다. 인간이 합성한 다이아몬드를 비롯해 여러 가지 결정들은 자연산이 아니기 때문에 엄밀한 의미에서 광물이라 부를 수 없다. 세 번째는 일정한 화학조성을 가져야 한다. 이 것은 항상 고정된 화학 조성을 가져야 한다는 의미는 아니다. 화학 조성이 어떤 범위의 값을 가질 수도 있지만, 무작위 값을 가져서는 광물이라 부를 수 없다. 광물이 되기 위한 네 번째 조건은 일정한 내부 구조를 가져야 한다는 것이다. 내부 구조란 광물을 구성하고 있는 원자들의 결합에 따른 공간적 배열을 의미한다. 즉, 광물이 되기 위해서는 이 공간적 배열이 일정하여야 한다는 뜻이다. 이에 대한 설명으로 유리의 예를 들어보자. 유리는 우리 인간이 살아가는데 없어서는 안될 소중한 물건이다. 이 유리는 광물일까? 두 가지 점에 있어서 유리는 광물이 아니다. 우선 우리가 사용하는 유리는 사람이 만들었으므로 위 광물이 되기 위한 두 번째 조건 자연산이어야 한다는 것에 위배되므로 광물이 아니다. 또한 유리는 일정한 내부구조를 갖지 않는다. 그래서 광물이 아니다. 자연적으로 산출되는 유리도 있다. 바로 화산 폭발시 분출되는 화산재나 매우 급하게 식은 용암이 유리를 포함하고 있는데, 이 유리들은 자연산이지만 일정한 내부 구조를 갖지 못하므로 광물이 아니다. 광물이 되기 위한 마지막 조건은 당연히 고체이어야 한다는 것이다. 수은은 자연산으로 단일 원소형태로 산출되지만, 상온 상압에서 액체 상태이기 때문에 광물이 아니다. 위의 광물에 대한 정의는 매우 엄격한, 그래서 좁은 뜻(협의)의 광물에 대한 정의라고 한다. 우리는 대개 좀 더 넓은 뜻으로 광물이라는 용어를 사용한다, 위 조건 중 세 번째, 네 번째 그리고 마지막 조건을 만족하면 결정이라고 하는데, 이를 넓은 의미의 광물이라고 생각해도 무방하다. 광물은 아래와 같은 매우 다양한 방법으로 만들어진다:
이렇게 만들어진 광물 한 두 가지가 특별히 집중되어 나타나는 곳을 광상이라고 하며, 경제적으로 채광하여 광물 자원을 채취할 수 있는 대상이 된다. 광상에 대해서는 뒤에 조금 더 자세히 다루도록 하자. 2-1-2. 광물의 종류 광물은 주요 결합 성분에 따라 종류를 구분한다(표 2-1-1).
표 2-1-1. 광물의 종류
지각의 대부분을 구성하는 광물들은 Si-O 결합을 기본 뼈대로 하는 것들인데, 이러한 광물을 통칭해서 규산염광물(silicates)라고 한다.
규산염광물은 지각뿐만 아니라, 맨틀, 운석, 그리고 다른 행성들의 암석 부분을 이루는 주요 광물이다. 규산염 광물을 구성하는 Si은 네 개의
산소와 직접 결합하여 Si-O4 사면체를 이루며(그림 2-1-1) 산소는 두 개의 실리콘과 직접 결합하여 이 사면체 들을 연결한다.
규산염광물의 예로는 정장석(orthoclase), 투휘석(diopside), 투각섬석(tremoloite) 등이 있다(그림 2-1-2).
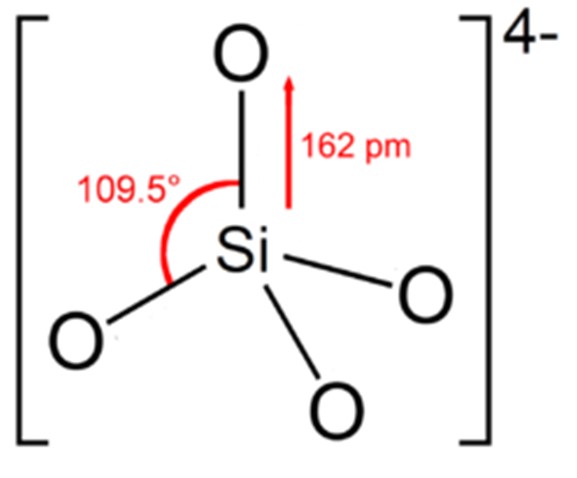 그림 2-1-1. SiO4 사면체. https://en.wikipedia.org/wiki/Silicate.
그림 2-1-2. 왼쪽부터 정장석, 투휘석, 투각섬석. 출처;차례대로 http://en.wikipedia.org/wiki/File:OrthoclaseBresil.jpg, http://en.wikipedia.org/wiki/File:Diopside_Aoste.jpg, http://en.wikipedia.org/wiki/File:Tremolite_Campolungo.jpg 위에 소개한 광물들의 결정은 모두 제 모습이 잘 갖춰져 있다. 하지만 실제로 자연에서는 이렇게 제 모습을 갖는 경우가 오히려 드물다. 왜냐하면 광물의 결정이 성장할 때 그 옆에 다른 결정이 같이 자라면서 서로 방해하기 때문이다. 집 근처의 산이나 들에 암석이 있으면 주어서 자세히 살펴보자. 아마도 암석이 입자들로 촘촘히 구성되어 있을 것이다. 이 각각의 입자가 다 광물 결정인데, 이들 중 제 모습을 갖춘 결정은 거의 없을 것이다. 규산염 광물 이외에도 많은 종류의 광물들이 있는데, 이들을 함께 묶어 비규산염광물(nonsilicates)라고 한다. 비규산염 광물 중 많은 수가 우리 주변에 흔히 발견된다. 비규산염 광물에는 산화광물, 수산화광물, 황산염광물, 탄산염광물, 인산염광물, 할로겐광물, 황화광물, 원소광물 등이 있다(표 2-1-1). 이들 광물의 구분은 이미 앞에서 설명하였듯이 결합을 이루고 있는 성분에 따라 하는데, 특히 음이온 성분에 따른다. 예를 들면 탄산염 광물은 모두 탄산기 CO3를 갖고 있으며, 이 음이온과 금속 양이온이 결합하여 광물을 만든 것이다. 탄산염 광물의 대표적인 광물인 방해석은 그 화학식이 CaCO3인데, CO32-가 Ca2+와 결합한 광물이다. 다른 광물들도 어떤 음이온들과 결합하고 있는지 살펴보기 바란다. 표 2-1-1에 기술한 광물 이외에 더 많은 종류의 광물들이 있으나, 광물의 종류에 대한 소개는 여기서 마치기로 하자. 이 강의의 목표는 광물은 무엇이고, 어떤 종류가 있으며, 어떻게 이용하고 그에 따라 어떠한 환경 문제가 있을 수 있는지를 이해시키는 것이므로, 이 정도 수준의 소개로 충분하다고 생각한다. 지금부터는 각 광물의 종류별로 대표적인 광물의 결정들을 살펴보고 이들이 어떻게 활용되는지 간단히 알아보자.
그림 2-1-3. 위 왼쪽부터 적철석(http://en.wikipedia.org/wiki/File:Hematite.jpg), 깁사이트(http://en.wikipedia.org/wiki/File:Gibbsite), 석고(http://en.wikipedia.org/wiki/Gypsum), 방해석(http://en.wikipedia.org/wiki/File:Calcite-HUGE.jpg), 아래 왼쪽부터 인회석(http://en.wikipedia.org/wiki/File:Apatite_crystals.jpg), 암염(http://en.wikipedia.org/wiki/File:Selpologne.jpg), 황철석(http://en.wikipedia.org/wiki/File:2780M-pyrite1.jpg), 금(http://en.wikipedia.org/wiki/Gold. 2-1-3. 광물의 이용
표 2-1-2. 광물의 분야별 이용 예.
광물은 거의 모든 산업 분야에서 이용된다고 해도 과언이 아니다. 위 표 2-1-2에 표시된 것은 그저 이렇게 다양한 분야에서 광물이 필수불가결하게
이용된다는 것을 보여주기 위한 것이며, 실제로는 훨씬 더 많은 분야에서 더 다양하게 이용되고 있다.
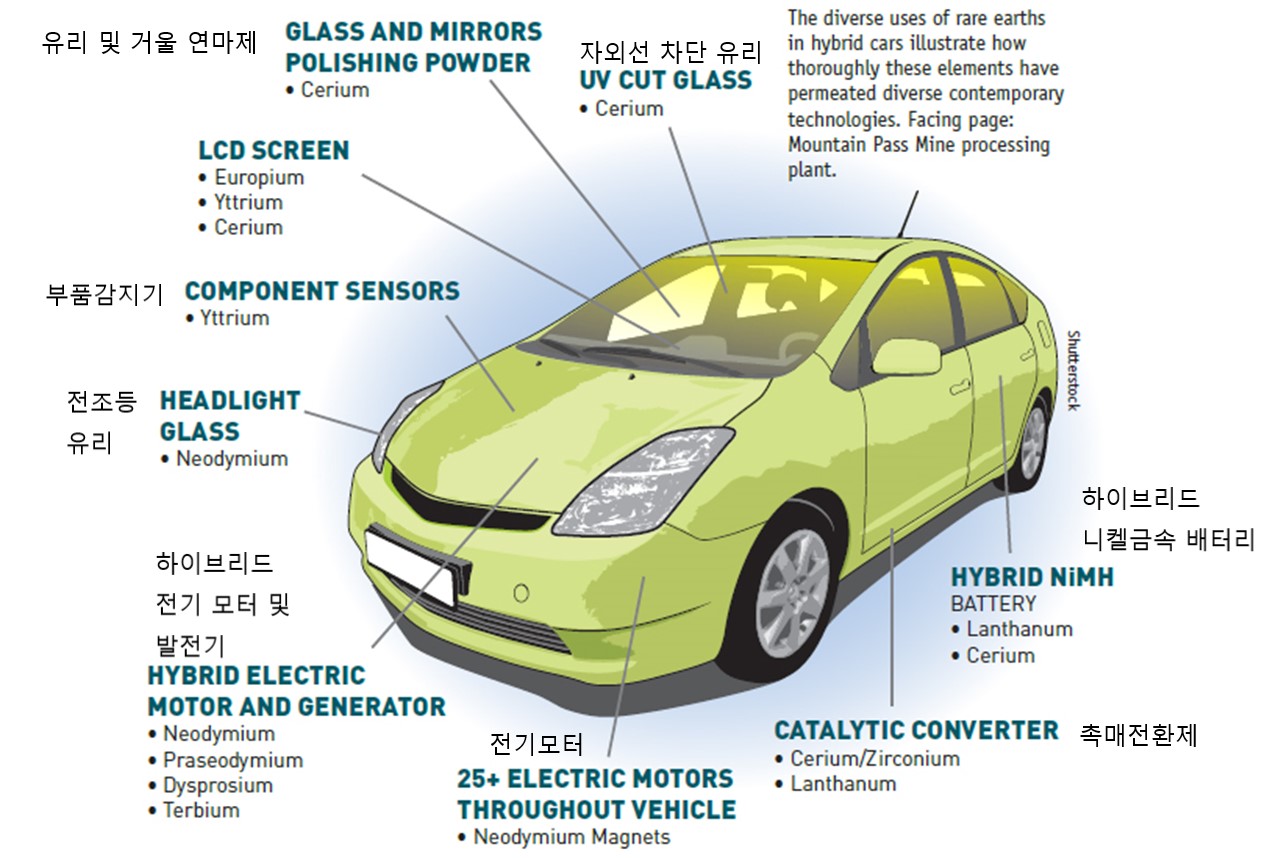
얼마 전 중국은 일본과의 영토 분쟁 때문에 보복 차원에서 일방적으로 일본으로의 희토류(REE; Rare Earth Elements) 자원 수출을 금지하였다. 당시는 물론 현재도 중국은 희토류 최대생산국이고, 일본은 아시아 최대 소비국이다. 잠시 동안이지만 일본은 이로 인해 여러 가지 제품 생산에 어려움을 겪었다. 희토류는 첨단 제품의 생산에 많지는 않지만 반드시 들어가는 재료이다. 희토류 성분이 구체적으로 어떻게 쓰이는 지 그림 2-1-4의 자동차의 예를 자세히 살펴보자. 그림에 표시된 것 이외에도 매우 많은 부위에 희토류 성분을 사용한다. 이러한 희토류 성분은 광물로부터 추출한다. 희토류 성분을 풍부하게 포함하고 있는 광물을 희토류광물(REE minerals)이라고 하는데, 희토류 광물에는 aschynite, allanite, apatite, abBastnasite, britholite, brockite, cerite, fluocerite, fluorite, gadolinite, monazite, parisite, stillwellite, synchisite, titanite, wakefieldite, xenotime, zircon 등이 있다. 그림 2-1-5는 미국에서 매년 일인당 사용하는 광물의 양을 그림으로 표현한 것이다. 국민 한사람에게 일상 생활이 가능하도록 매년 새로 공급해주어야 하는 광물의 양은 38,052파운드이다 (1파운드는 약 0.454kg입니다). 이 중에는 164파운드의 점토광물, 332파운드의 비금속광물, 8,509파운드의 일반 암석 광물, 5,599파운드의 모래 자갈 광물, 6파운드의 아연, 65파운드의 알루미늄 등이 포함된다. 대부분의 사람들은 보석을 좋아한다. 보석 역시 광물이다. 그림 2-1-6은 대표적인 보석인 탄생석을 나타낸 것이다. 각각 자신의 탄생석을 찾아보고, 그 보석이 의미하는 바가 무엇인지 알아보자. 2-2. 암석에 계속 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 차례 | 제 1장 | 제 2장 | 제 3장 | 제 4장 | 제 5장 | 제 6장 | 제 7장 | |